Hepatotoxicidad inducida por glucosamina-condroitina en un hospital público de Lima (Perú): reporte de un caso
DOI:
https://doi.org/10.22516/25007440.325Palabras clave:
glucosamina, condroitina, toxicidad, transaminasas, osteoartritisResumen
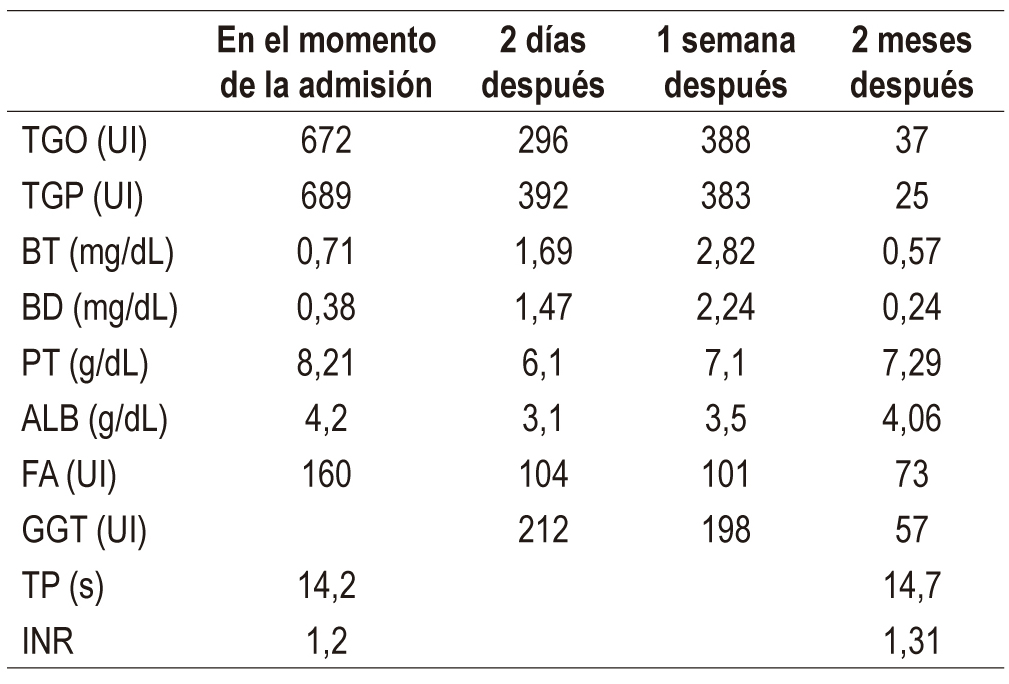
En el cuerpo humano tenemos glucosamina y condroitina de forma natural. Estas sustancias constituyen un componente importante del sistema cartilaginoso. Como medicamentos, tienen múltiples indicaciones clínicas, principalmente la osteoartritis. La hepatotoxicidad inducida por estas biomoléculas es infrecuente, pues cuentan solo con reportes de casos aislados en la literatura mundial. En este trabajo, presentamos el caso de una paciente con una lesión hepática inducida por glucosamina-condroitina del tipo hepatocelular, que fue admitida en el hospital por causa de una sintomatología respiratoria y malestar general. En ella, se destacó una marcada hipertransaminasemia durante los exámenes de laboratorio. Asimismo, se descartaron etiologías como el alcohol, hepatitis virales y hepatopatías autoinmunes, principalmente. De igual forma, no se llegó a evidenciar una enfermedad hepática crónica mediante la ecografía abdominal. Al suspenderse el medicamento, se observó una disminución considerable de la hipertransaminasemia luego de 1 semana, y una mejoría total de esta a los 2 meses del alta hospitalaria. Este caso se añade a los pocos reportados a nivel mundial y cobra una importancia relevante para la publicación de posteriores estudios sistemáticos que aclaren el panorama de esta enfermedad.
Descargas
Referencias bibliográficas
Ministerio de Salud. Informe técnico N° 22-2007: glucosamina sulfato 1,5 g/condroitina 1,2 g (polvo). Lima: Dirección General de Medicamentos, Insumos y Drogas; 2007.
Hochberg MC, Martel-Pelletier J, Monfort J, Möller I, Castillo JR, Arden N, et al. Combined chondroitin sulfate and glucosamine for painful knee osteoarthritis: a multicentre, randomised, double-blind, non-inferiority trial versus celecoxib. Ann Rheum Dis. 2016;75(1):37-44. http://dx.doi.org/10.1136/annrheumdis-2014-206792
Sawitzke AD, Shi H, Finco MF, Dunlop DD, Harris CL, Singer NG, et al. Clinical efficacy and safety of glucosamine, chondroitin sulphate, their combination, celecoxib or placebo taken to treat osteoarthritis of the knee: 2-year results from GAIT. Ann Rheum Dis. 2010;69(8):1459-64. http://dx.doi.org/10.1136/ard.2009.120469
Smith A, Dillon J. Acute liver injury associated with the use of herbal preparations containing glucosamine: three case studies. BMJ Case Rep. 2009;2009. pii: bcr02.2009.1603. https://doi.org/10.1136/bcr.02.2009.1603
Ebrahim V, Albeldawi M, Chiang DJ. Acute liver injury associated with glucosamine dietary supplement. BMJ Case Rep. 2012;2012. pii: bcr2012007665. https://doi.org/10.1136/bcr-2012-007665
Yang L, Aronsohn A, Hart J, Jensen D. Herbal hepatoxicity from Chinese skullcap: A case report. World J Hepatol. 2012;4(7):231–233. https://doi.org/10.4254/wjh.v4.i7.231
Linnebur SA, Rapacchietta OC, Vejar M. Hepatotoxicity associated with chinese skullcap contained in Move Free Advanced dietary supplement: two case reports and review of the literature. Pharmacotherapy. 2010;30(7):750, 258e-262e. https://doi.org/10.1592/phco.30.7.750
Ossendza RA, Grandval P, Chinoune F, Rocher F, Chapel F, Bernardini D. Acute cholestatic hepatitis due to glucosamine forte. Gastroenterol Clin Biol. 2007;31(4):449-50. https://doi.org/10.1016/S0399-8320(07)89410-3
Ip S, Jeong R, Schaeffer DF, Yoshida EM. Unusual case of drug-induced cholestasis due to glucosamine and chondroitin sulfate. World J Hepatol. 2015;7(24):2559–2562. https://doi.org/10.4254/wjh.v7.i24.2559
Cerda C, Bruguera M, Parés A. Hepatotoxicity associated with glucosamine and chondroitin sulfate in patients with chronic liver disease. World J Gastroenterol. 2013;19(32):5381-4. https://doi.org/10.3748/wjg.v19.i32.5381
Fransen M, Agaliotis M, Nairn L, Votrubec M, Bridgett L, Su S, et al. Glucosamine and chondroitin for knee osteoarthritis: a double-blind randomized placebo-controlled clinical trial evaluating single and combination regimens. Ann Rheum Dis. 2015;74(5):851-8. https://doi.org/10.1136/annrheumdis-2013-203954
Bruyère O, Altman RD, Reginster JY. Efficacy and safety of glucosamine sulfate in the management of osteoarthritis: Evidence from real-life setting trials and surveys. Semin Arthritis Rheum. 2016;45(4 Suppl):S12-7. https://doi.org/10.1016/j.semarthrit.2015.11.011
Clegg DO, Reda DJ, Harris CL, Klein MA, O’Dell JR, Hooper MM, et al. Glucosamine, chondroitin sulfate, and the two in combination for painful knee osteoarthritis. N Engl J Med. 2006;354(8):795-808. https://doi.org/10.1056/NEJMoa052771
de Vos BC, Landsmeer MLA, van Middelkoop M, Oei EHG, Krul M, Bierma-Zeinstra SMA, et al. Long-term effects of a lifestyle intervention and oral glucosamine sulphate in primary care on incident knee OA in overweight women. Rheumatology (Oxford). 2017;56(8):1326-1334. https://doi.org/10.1093/rheumatology/kex145
LiverTox: Clinical and Research Information on Drug-Induced Liver Injury [Internet]. Bethesda (MD): National Institute of Diabetes and Digestive and Kidney Diseases; 2012. Glucosamine. [actualizada el 12 de marzo de 2020]. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK547949/
Descargas
Publicado
Cómo citar
Número
Sección
Licencia
Aquellos autores/as que tengan publicaciones con esta revista, aceptan los términos siguientes:
Los autores/as ceden sus derechos de autor y garantizarán a la revista el derecho de primera publicación de su obra, el cuál estará simultáneamente sujeto a la Licencia de reconocimiento de Creative Commons que permite a terceros compartir la obra siempre que se indique su autor y su primera publicación en esta revista.
Los contenidos están protegidos bajo una licencia de Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional.


| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |